罕见病又称“孤儿病”,一般指患病率低于五十万分之一,或新生儿发病率低于万分之一的疾病,其发病率虽低,但病种很多。目前,国际确认的罕见病有7000多种,例如白血病、“瓷娃娃”、“渐冻症”,但还有很多鲜为人知的罕见病。研究显示,80%以上的罕见病与遗传因素有关。胚胎植入前遗传学检测(PGT)是针对遗传性染色体病和单基因病的胚胎检测技术,帮助将健康的胚胎植入母体,从而达到阻断致病基因传递,生育健康后代的目的。
2021年7月17日,在中华医学会北京分会举办的2021年北京围产医学学术会议上,北京大学第三医院生殖医学中心朱小辉教授详细讲解了PGT联合HLA配型技术在脐带血临床治疗中的应用,现对讲座内容进行整理,与读者分享。
“罕见病”是指流行率很低、很少见的疾病。根据世界卫生组织(WHO)的定义,罕见病为患病人数占总人口的0.65‰~1‰的疾病。世界各国及各地区对罕见病的认定标准存在一定的差异。例如,美国将罕见病定义为每年患病人数少于20万人(或发病人口比例小于1/1500)的疾病;日本规定,罕见病为患病人数少于5万(或发病人口比例为1/2500)的疾病,中国台湾则定义为患病率低于1/10000,由基因缺陷引起且很难诊断或治疗的疾病。
据统计,目前已知的罕见病超过7000种,约占人类疾病的10%,全球受累人数超过3亿,我国受累人数超2000万,每年新增约20万例。大约有50%的罕见病在新生儿或儿童期发病、致畸致残甚至致死,并且治疗方法很少,给社会和家庭带来沉重的负担。
研究显示,80%以上的罕见病由遗传因素导致,50%在出生或儿童期发病。一旦配偶双方存在相同的缺陷基因,下一代就有可能患罕见病。遗传病包括很多种类型,比如染色体病、单基因遗传病、多基因遗传病、线粒体遗传病以及遗传性肿瘤等等,具体如下图。
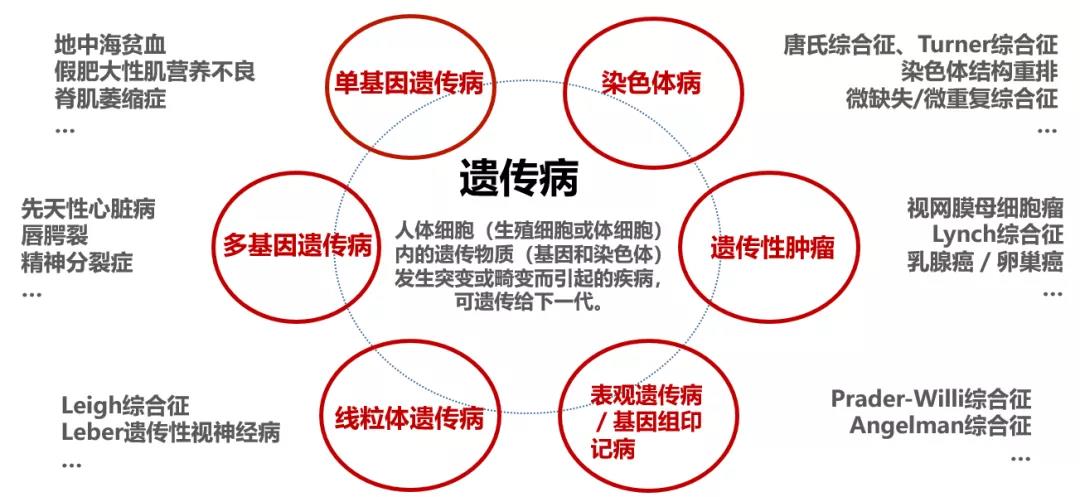
PGT是针对遗传性染色体病和单基因病的胚胎检测技术,包括染色体非整倍性PGT(PGT-A)、染色体结构重排PGT(PGT-SR)、单基因病PGT(PGT-M)、人类白细胞抗原PGT(PGT-HLA)。
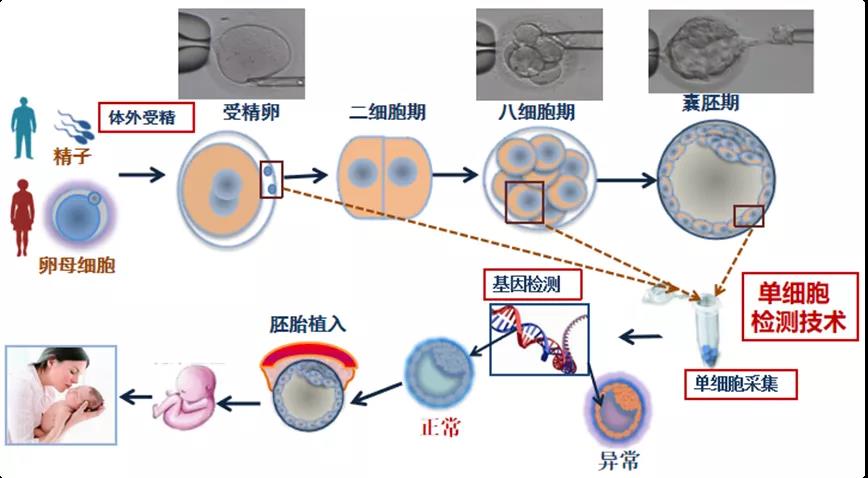
通过PGT技术,可以将不会患家族性遗传病的胚胎植入母体,从而达到阻断致病基因传递,生育健康后代的目的。它为携带明确的染色体变异或致病基因突变的遗传家系带来生育健康宝宝的希望,大大减少了传统孕中期产前诊断后孕妇可能需要的引产,极大减轻了随之而来的身心痛苦。
患者在进入试管流程前,建议进行遗传咨询和专科咨询,了解家族遗传病和致病基因,以及干细胞移植对患儿治疗是否可行。入组以后对致病基因变异在家系成员中进行验证,患者就可以进入试管周期,接受超促排卵。取卵后体外受精,待胚胎发育到第5~6天囊胚期,活检少数囊胚期滋养层的细胞(将来发育成胎盘的部分),用于遗传学检测。之后选择不患病的胚胎移植,移植妊娠后,中期再进行一次产前诊断,最大限度保障健康宝宝的出生。新生儿出生以后还要注意随访,建立一套完善的儿童保健流程。
人类白细胞抗原(HLA)基因簇位于6号染色体短臂,分为I、II、III类,其中I类和II类基因产物(抗原)直接参与移植免疫反应,III类抗原起间接作用。一般认为,HLA-A、B和 DR与造血干细胞移植关系最为密切,具有高度多态性,是已知人类最复杂的多态系统。
某些疾病的患儿需要移植造血干细胞进行治疗,PGT结合HLA分型可以帮助这些家庭孕育健康的宝宝,同时通过移植PGT新生儿的脐带血干细胞来治愈患儿。
基于NGS技术的HLA-SNP连锁分型方法是指在生物信息学分析过程中,以先证者为依据,HLA基因内及基因附近SNP连锁区分父母源单体型,进而比对胚胎携带的HLA单体型和先证者是否一致。这一新策略可以诊断单基因遗传病、诊断HLA相合情况、筛查染色体非整倍性,适用于各种遗传病家系,并且HLA分型分辨率高,只需一次测序反应,具有简便、高效、低成本的优点。

2018年7月,一对夫妻来到北京大学第三医院生殖医学中心求助。他们的第一个宝宝在2016年10月出生,主要症状包括肋外翻、关节软、易摔跤、脊柱右侧弯、骨发育不良。基因检测后,确诊患儿罹患黏多糖贮积症4型,致病基因为GALNS。在上海和台湾咨询后,告知可以采用骨髓移植或干细胞移植的方法治疗,但苦于找不到与患儿相合的骨髓源。配型全相合的同胞脐带血,无痛采集,实物储存,可在最短的时间内提供给临床用于治疗,并且移植后排异反应少,酶活性高,是此例患儿最佳的移植用造血干细胞来源。
北京大学第三医院生殖医学中心采取基于NGS的SNP分型策略(一次构建DNA文库、一次高通量测序),结合PGT技术,顺利为患儿母亲移植一枚健康胚胎,经胎儿羊水检测,与患儿HLA配型全合。健康二宝于2019年9月20出生,北京大学第三医院产科在胎儿出生断脐后随即采集脐带血。
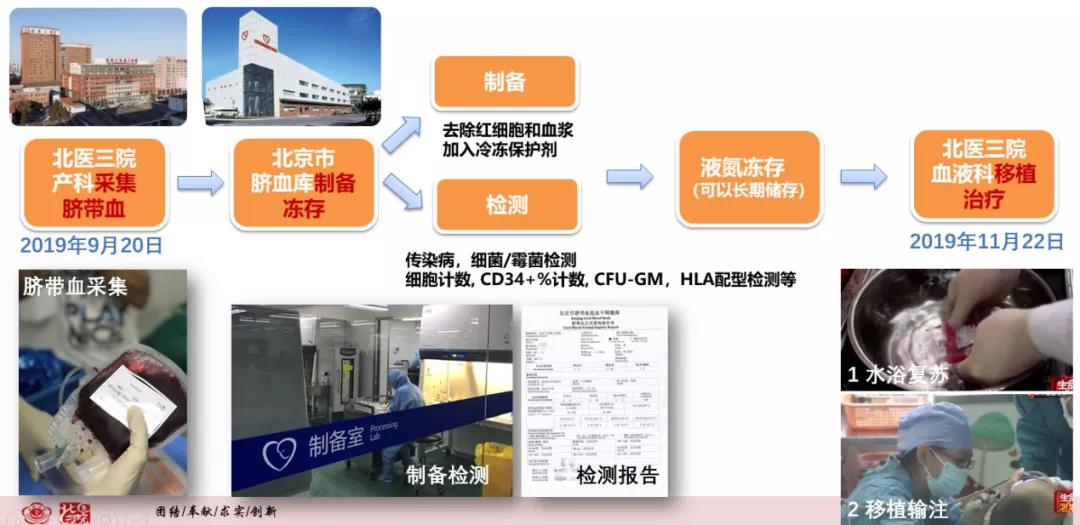
脐带血采集完成后,由北京市脐血库的取血人员运送回库,进行制备、冻存和检测工作。制备和冻存过程去除脐带血中的红细胞和血浆,并加入冷冻保护剂,通过计算机控制逐步降温,然后放入液氮深低温保存。检测主要是对病原微生物、造血干细胞的功能和数量等进行检测。最终所有检测合格的脐带血可以在液氮中长期保存。目前,北京市脐血库已解冻过多份保存20余年的脐带血,在复苏后,造血干细胞活性达到90%以上,可以满足临床应用的需求。
在医院为患儿做好移植准备后,脐血库在约定好的时间将脐带血送至医院血液科,经过快速水浴解冻后,直接通过静脉输入患儿体内。脐带血移植几个月后,大宝的酶学水平恢复正常,通过脐带血造血干细胞移植得到成功的治疗。
目前,北京大学第三医院生殖医学中心PGT团队在乔杰院士的带领下,已入组737个家系,覆盖200余种遗传病,通过胚胎植入前的单基因遗传学检测(PGT-M),已帮助137个健康的宝宝出生。他们也在不断地探索和创新,已实现单基因联合染色体病诊断、单基因联合HLA分型、多个基因同时诊断等等复杂情况的胚胎植入前遗传学诊断。
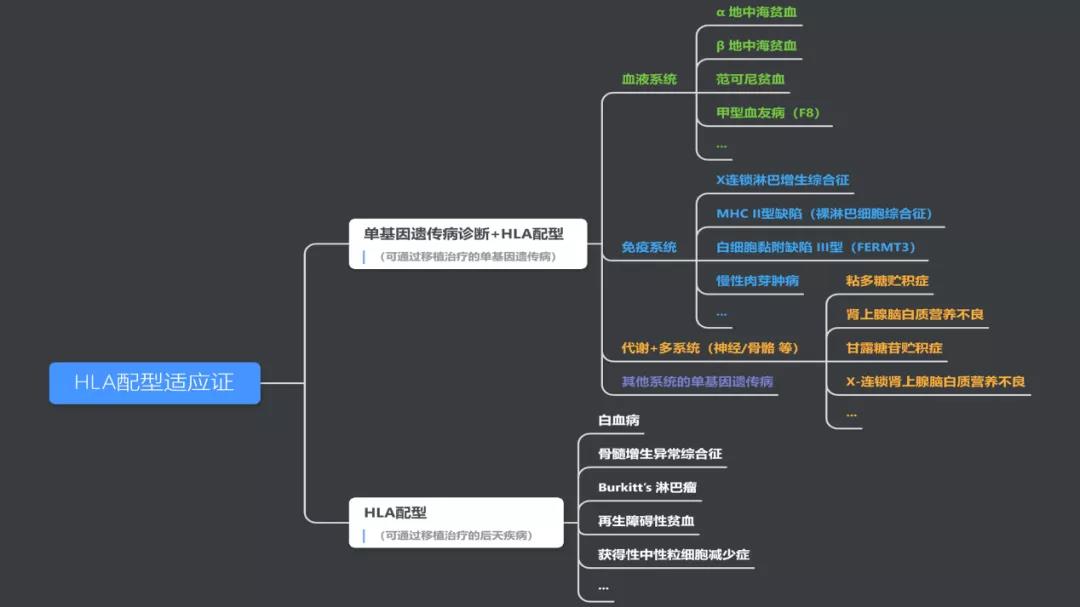
朱小辉教授讲到,PGT-HLA的适应证包括可通过造血干细胞移植治疗的单基因病和可通过造血干细胞移植治疗的后天疾病等。PGT-HLA具有时效性,要考虑患儿疾病进展、母亲年龄和IVF适应证,同时还需要多学科合作,包括临床生殖中心、产科、血液科、儿科和脐血库的全方位支持。希望该技术可以在临床上得到更大范围的应用,惠及更多的家庭!
文章来源:妇产科在线